
2019년 10월 식약처는 「의료기기법 시행규칙」을 개정하여 의료기기 제조.수입업체 및 의료기관 대상으로 국내에 유통하는 의료기기 공급 정보를 확인하기 위하여 공급내역 보고 제도를 실시했습니다.
의료기기 공급내역보고 대상이 등급별로 시행일이 다르고 중간 중간 변동 사항이 있었던 만큼 혼선이 따를 수 밖에 없습니다. 특히 올해 7월에도 의료기기 공급내역보고에 관해 일부 개선 사항이 있었습니다.
오늘은 의료기기 공급내역보고 대상 업체와 보고 방법에 대해서 말씀드리겠습니다.

의료기기 공급내역보고 대상 업체
□ 의료기기 공급내역보고 대상 업체
1. 모든 의료기기 제조.수입 업체
2. 의료기관에 유통하는 모든 의료기기 도.소매 업체
※ 소매업체에서 일반인에게 판매하는 의료기기 건에 대해서는 공급내역 보고 대상이 아님
※ 소매업자가 의료기관에 유통하는 치료재료는 공급내역 중 공급가격을 추가로 보고해야함

의료기기 공급내역 보고 방법
의료기기 공급내역 보고서는 매월 말일까지 작성해서 제출합니다.
의료기기 공급내역보고는 의료기기통합정보시스템 (https://udiportal.mfds.go.kr/)
사이트에서 공급내역관리란을 통해 진행합니다.
□ 작성방법

공급자의 영업형태 : 제조업자, 판매업자, 수입업자, 임대업자
공급 구분 : 출고(임대 제외), 반품(임대 제외), 폐기, 임대, 회수
공급 형태
1. 제조, 수입, 판매, 임대업자에게 공급한 경우
2. 의료기관에 공급한 경우
3. 약국개설자 또는 의약품도매상에게 공급한 경우
4. 견본품, 기부용 또는 군납용으로 공급한 경우
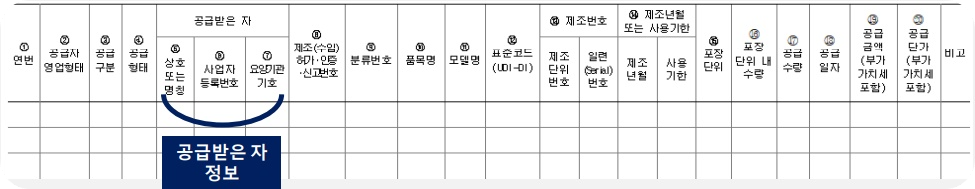
공급받은 자 : 의료기기를 공급받은 자의 정보를 기재
상호 또는 명칭, 사업자등록번호(제조, 수입, 판매, 임대, 의료기관), 요양기관 번호(공급받은 자가 의료기관인 경우)

표준코드 및 제품정보
표준코드 UDI-DI : 공급한 의료기기의 고유식별자
제조번호 : 제조단위번호 또는 일련번호 (시리얼 넘버)
※제조,수입업체에서 관리하는 제조단위번호 또는 일련번호를 기재함
제조년월 또는 사용기한
공급한 의료기기의 제조년월 또는 사용기한으로 용기 등의 기재사항과 동일함
포장단위 : EA, BOX 등
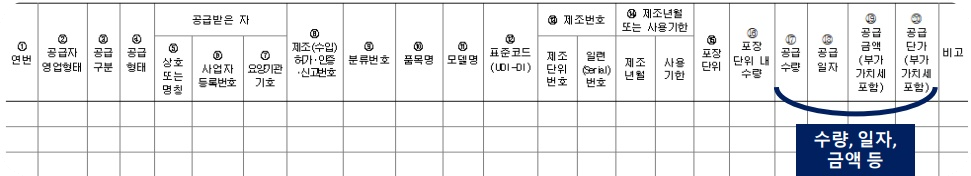
공급수량 : UDI 기준 공급한 의료기기의 총 수량
공급일자 : 창고에서 나가는 날을 기준으로 일자 기재
공급금액 및 단가
대상 : 요양급여 치료재료에 해당하는 의료기기
(「국민건강보험 요양급여의 기준에 관한 규칙」 제8조 제2에 따라 고시된 치료재료)
공급받은 자 : 의료기관에 공급한 경우
보고 내용 : 거래명세서 단위별로 부가가치세를 포함한 금액 기재
의료기기통합정보 관리책임자 지정
의료기기통합정보를 효율적이고 체계적으로 관리하기 위하여 의료기기통합정보 관리책임자를 두도록 하고 있습니다.
표준코드 및 공급내역보고 관련 절차 및 문서에 관리책임자가 지정 되어 있음을 확인할 수 있어야 합니다.
관리책임자는 의료기기통합정보관리기준에 따라 업무를 수행하고 있는지 종사자를 점검.확인하는 권한을 가지고 업체 내에서 겸임할 수 있습니다.
아울러 품질책임자가 관리책임자를 겸직할 수 있으므로 별도 채용은 필요 없습니다.

위반시 행정처분
의료기기 공급내역보고는 의료기기를 공급한 달을 기준으로 그 다음 달 말일까지 의료기기통합정보시스템에 제출해야 합니다.
다시말해, 매월보고하는 것이 원칙입니다.
Ex) 23년 3월 1일부터 31일까지 공급한 의료기기 건에 대해서는 4월 30일까지 의료기기통합정보시스템에 보고합니다.
그렇지 않은 경우 위반에 따른 행정처분이 있습니다.
|
구분
|
제조.수입업자
|
판매.임대업자
|
|
공급내역 보고 기한이 경과된 날부터 1개월 이내에 보고한 경우
|
해당 품목 판매 업무 정지 15일
|
판매.임대 업무 정지 7일
|
|
공급내역 보고 기한이 경과된 날부터 1개월 이내에 보고하지 않은 경우
|
해당 품목 판매 업무 정지 1개월
|
판매.임대 업무 정지 15일
|
|
거짓으로 보고한 경우
|
해당 품목 판매 업무 정지 1개월
|
판매.임대 업무 정지 15일
|
※ 「의료기기법 시행규칙」 별표8, 1차 위반 기준

이상으로 의료기기 공급내역보고 대상 업체와 방법에 대해서 말씀드렸습니다.
식약처에서 제조.수입.판매.임대 업체 대상으로 표준코드 및 공급내역보고에 관한 모니터링을 지속적으로 하고 있습니다.
신규업체라서 잘 몰랐다는 이유로 기간 내에 보고를 하지 못한 경우라도 위반시 행정처분이 따르므로 기간 내에 표준코드(UDI) 생성 및 의료기기 공급내역보고 잘 하셔야 겠습니다.
저희 다림행정사사무소에서는 의료기기 신고, 인증, 허가 업무를 대행하고 있습니다.
업무 의뢰 및 대행이 필요하시다면 언제든지 연락주세요.
'의료기기인허가(인체, 동물용)' 카테고리의 다른 글
| 동물용의료기기 기술문서 작성법 2탄 (제조방법, 성능 및 사용목적, 포장단위, 저장방법 또는 사용기한) 예시 포함 (1) | 2023.09.01 |
|---|---|
| 동물용의료기기 기술문서 작성법 1탄 (제품명, 외형, 원재료) (1) | 2023.08.25 |
| 동물용의료기기 수입 허가(신고) / 허가 신고 대상 확인 방법 / 신청 서류 작성 요령 (0) | 2023.08.12 |
| 의료기기UDI 생성 방법 / 의료기기 표준코드 / 의료기기 인허가 이후 절차 안내 (0) | 2023.08.06 |
| 의료기기 인허가 의료기기 기술문서 원재료 작성 가이드라인 개정 (1) | 2023.07.27 |